实验描述
(1)实验教学过程
本实验共有12学时,实验教学过程主要是通过引导学生思考与研究的探究式教学模式进行设计的。整个实验共分为四个大模块,其中第一模块2学时,第二模块3学时,第三模块4学时,第四模块3学时。
整个虚拟仿真实验是以学生自主操作为主,指导教师讲解实验过程及方法为辅助的一种实验教学方法。利用计算机模拟实验操作,完成细胞培养、外泌体的分离、外泌体的鉴定与外泌体的靶向修饰四大模块的操作。在实验开始前,学生进行自主学习,初步了解实验的原理与目的,了解整个实验的大体框架,然后由指导老师进行具体的实验步骤讲解,让学生了解每一步骤要点,之后给与时间让学生互相讨论交流。然后让学生进行实验模拟操作,具体在软件上体会课堂讲解的每一步的操作要点,在此过程中老师影只起到引导与推动的作用,让学生深刻体会各项实验的操作要点。最后老师要让学生总结实验过程中遇到的难点问题,提交实验报告。
这个虚拟仿真实验共分为四大模块,具体实验流程如下图:
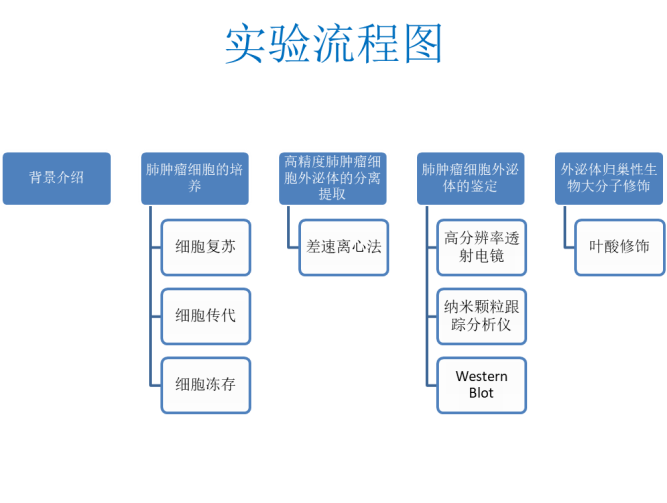
模块一:肺肿瘤细胞的培养(2学时)
(1)细胞复苏
1)液氮中取出A549细胞冻存管,37℃水浴,迅速摇动至完全融化,75%酒精消毒移至超净工作台;
2)将冻存管中细胞悬液取出转移至15ml离心管中,300g离心5min,去上清;
3)将含沉淀的离心管中加入5ml含10%去外泌体血清的DMEM完全培养基,将细胞重悬,轻轻吹打使其分散,转移至细胞培养瓶中并使其在培养瓶中均匀分布,在细胞培养瓶表面标记培养信息,置于37 ℃,5%湿润CO2培养箱中培养;
4)利用倒置显微镜观察细胞的生长状态,当细胞铺满瓶壁的80%时,进行细胞传代,更换培养液,继续培养48h,收集细胞培养上清液,用于外泌体的提取。
(2)细胞传代
1)在超净工作台中将细胞培养瓶内的培养基弃去,使用无菌的胶头滴管吸取一管磷酸盐缓冲液(PBS)并沿无细胞一侧的瓶壁缓缓加入到细胞培养瓶中,轻轻摇动培养瓶将死细胞以及代谢物清洗掉,重复洗三次;
2)使用另一只无菌胶头滴管吸取一管无菌0.25%胰酶消化液,沿无细胞一侧的瓶壁缓缓加入到细胞培养瓶中,静置消化,在倒置显微镜下观察到细胞变圆后,倒出消化液,加入适量培养液终止消化;
3)使用无菌弯头吸管,吸取瓶内的培养基,反复吹打培养瓶壁上的细胞,直至全部垂落下来,再轻轻地吹打细胞悬液,使其彻底分散,最后对细胞悬液进行分装处理,分装好的细胞培养瓶上做好标记,将其放入CO2培养箱之前,先轻轻摇匀瓶内的细胞悬液,使细胞均匀生长。
(3)细胞冻存
1)利用倒置显微镜观察细胞的生长状态,当细胞铺满瓶壁的80%时,在超净工作台中将细胞培养瓶内的培养基弃去,使用无菌的胶头滴管吸取一管磷酸盐缓冲液(PBS)并沿无细胞一侧的瓶壁缓缓加入到细胞培养瓶中,轻轻摇动培养瓶将死细胞以及代谢物清洗掉,重复洗三次;
2)使用另一只无菌胶头滴管吸取一管无菌0.25%胰酶消化液,沿无细胞一侧的瓶壁缓缓加入到细胞培养瓶中,静置消化,在倒置显微镜下观察到细胞变圆后,倒出消化液,加入5ml培养液终止消化;
3)使用无菌弯头吸管,吸取瓶内的培养基,反复吹打培养瓶壁上的细胞,直至全部垂落下来,再轻轻地吹打细胞悬液,使其彻底分散,转移至15ml无菌离心管中,300g离心5min;
4)离心管弃上清,超净台中加入5ml磷酸盐缓冲液(PBS)重悬细胞,300g离心5min;
5)离心管弃上清,按2X106个细胞加入1ml冻存液(90%DMEM完全培养基+10%DMSO)的比例重悬细胞;
6)在超净台中将1ml细胞冻存液转移至容积为2ml的细胞冻存管中,按4℃,30min,-20℃,30min,-80℃过夜的程序梯度缓慢降温,并于次日放入液氮罐中长期冻存;
模块二:高精度肺肿瘤细胞外泌体的分离提取(3学时)
(1)利用倒置显微镜观察细胞的生长状态,当细胞铺满瓶壁的80%时,更换新的DMEM培养液,继续培养48h,收集细胞培养上清液,用于外泌体的提取;
(2)取细胞上清于无菌50ml离心管中4℃,300g离心10min,目的去除游离细胞;
(3)取上清于无菌50ml离心管4℃,2000g离心10min,目的去除死亡细胞;
(4)取上清于无菌50ml离心管4℃,10000g离心30min,目的去除细胞碎片;
(5)取上清,使用无菌50ml注射器过0.22μm微孔滤膜,目的除去离心后残留的大颗粒;
(6)将离心后的培养基转入超速离心机专用的离心管中,超速离心4℃,100000g离心70min,小心吸去上清,沉淀中含外泌体和一些杂蛋白;
(7)使用无菌预冷的PBS溶液轻轻吹打均匀使沉淀复溶,再次置于超速离心机专用离心管4℃,100000g离心70min,小心吸去上清,沉淀用无菌预冷的PBS重悬,轻柔吹打均匀使沉淀复溶,即得纯化外泌体,将其转移至无菌EP管中,-80℃冰箱长期保存。
模块三:肺肿瘤细胞外泌体的鉴定(4学时)
(1)高分辨率透射电镜
1)制样 取上述外泌体悬液10μL,滴加到200目碳膜铜网上,常温静置15min,使用滤纸小心吸取剩余液体,将3%磷钨酸溶液滴于铜网上,负染10min,使用滤纸将多余负染液吸去,室温静置晾干;
2)上机观察 将铜网置于透射电镜样品室对外泌体形态进行观察。
(2)纳米颗粒跟踪分析仪
将上述超速离心样品使用超纯水稀释1000倍,充分,温柔地混合均匀,使用吸管将样品加入至样品池中使用纳米颗粒跟踪分析仪ZetaView检测粒径大小。
(3)Western Blot
1)试剂的配置
TBST缓冲液、BSA封闭液、SDS-PAGE电泳缓冲液、转膜缓冲液。
2)胶的配置
先配15%分离胶迅速加入胶板中使之到刻度,待其凝固后,将水倒出,再配制5%浓缩胶,迅速加入胶板中,并插入梳子待其凝固。
3)制样
取超速离心所得的外泌体悬液,加入PMSF,使其终浓度为1mM,再加入适量RIPA细胞裂解液,混合均匀,冰浴裂解30min,之后4℃离心10000g离心15min,取上清得到外泌体总蛋白,采用BCA蛋白定量试剂盒对外泌体裂解液进行蛋白定量,1:1加入SDS-PAGE上样缓冲液,混合均匀, 100℃,煮沸10min,即得上样样品。
4)SDS-PAGE蛋白电泳
将梳子拔出,将仪器说明书组装好电泳系统,内槽中加入SDS-PAGE电泳缓冲液,使用移液器吸取10μL蛋白Marker,加至胶孔中,样品也依次加至胶孔中,组装完电泳仪,以80V恒压进行电泳,待溴酚蓝指示剂移至电泳槽底部,停止电泳,取出玻璃板,小心剥下凝胶,参照蛋白Mark,切取目标蛋白所在的条带。
5)转膜
小心剪切PVDF膜,使膜的大小与所切胶的大小相当,将其侵入甲醇中20s左右进行激活,去离子水漂洗后放入转膜缓冲液备用,转膜缓冲液清洗转膜槽,将转膜夹子阴极置于最下方,依次放入转膜缓冲液浸湿浸透的海绵垫、转膜缓冲液浸湿浸透的三层定性滤纸、切割的目标蛋白所在的凝胶,形成PVDF膜-转膜缓冲液浸湿浸透的三层定性滤纸、在转膜缓冲液浸湿浸透的海绵垫夹上阳极碳板,确保整个系统中没有气泡产生,将其放入电泳槽中,加入适量转膜缓冲液,使其没过转膜板。组装好转膜系统,100V,60min。
6)封闭
转膜完成后,将PVDF膜用TBST彻底洗干净后,将其置于盛有BSA封闭液的大平皿中,正面朝上,脱色摇床上室温封闭1h。
7)敷一抗
将封闭后的PVDF膜使用TBST彻底清洗干净,使用TBST将一抗按1:5000进行稀释,将PVDF膜置于孵育盒中,正面朝下,加入一抗使其没过PVDF膜,脱色摇床4℃孵育过夜。
8)敷二抗
将敷完一抗的PVDF膜在脱色摇床上使用TBST缓冲液清洗3次,每次15min,将二抗按1:10000进行稀释,将清洗好的PVDF膜置于盛有二抗稀释液的孵育盒中,脱色摇床上4℃孵育4h。
9)ECL化学发光,凝胶成像系统采集图像
经孵育完二抗的PVDF膜使用TBST缓冲液清洗3次,每次15min。ECL试剂盒中的A液、B液按1:1混匀,镊子将膜从TBST中取出,滤纸吸去多余的TBST,将膜的正面即蛋白面放入混合液中,摇床避光反应2min,取出膜,用滤纸将多余的混合液吸除,放入凝胶成像系统,设置化学发光信号检测模式,根据信号强弱适当调整曝光时间,获取清晰、完整的蛋白条带。
模块四:外泌体归巢性生物大分子(RNA、蛋白质)修饰(3学时)
(1)将超速离心制备的外泌体,使用PBS调整外泌体蛋白含量为50 mg/ml;
(2)取外泌体分散液2 ml,加入0.1 ml浓度为20 mg/ml的DSPE-PEG-FA溶液,用枪头轻轻吹打混匀,在室温下孵育1小时;
(3)之后将分散液在超净台中将其转移至超速离心机专用离心管,超速离心机4°C, 100000g离心70min;
(4)吸去上层溶液,去除未结合的DSPE-PEG-FA,所得沉淀即为连接了叶酸靶头的外泌体向沉淀中加入预冷的PBS溶液吹打使沉淀复溶即得叶酸靶头的外泌体。
二、实验方法
本实验主要是通过细胞培养、差速离心法、Western Blot等各种实验方法对外泌体的靶向修饰及归巢性的特性进行了初步研究。整个实验过程所涉及到的实验方法主要包括以下几个:
(1)通过细胞复苏,对A549肺癌细胞进行复苏,并使细胞长至80%左右进行传代培养,细胞用完结束后要对细胞进行冻存。这一步主要是培养肺癌细胞使其分泌外泌体至培养液中,收集细胞培养液,利用其进行外泌体的提取;
(2)通过差速离心法进行外泌体的提取,首先进行常规高速离心:300g在4℃离心10min,2000g在4℃离心10min,10000g在4℃离心30min;然后进行超高速离心:100000g在4℃离心70min,PBS重悬后100000g在4℃离心70min;
(3)通过透射电镜观察提取的外泌体的形态,主要呈现出茶托状结构;
(4)通过纳米颗粒跟踪分析仪测提取到的颗粒粒径大小,大约在30-150nm左右;
(5)通过Western Blot实验检测外泌体的标志蛋白CD63、CD9和TSG101的表达情况;
(6)通过共孵育的方法使其化学键相连实现外泌体的靶向修饰。